Осмотическая система очистки воды — лучшая на данный момент
Осмотическая система очистки воды на сегодняшний день считается самой прогрессивной и востребованной, у которой наивысшая степень очистки. Применение системы обратного осмоса позволяет удалить из воды до 99-ти процентов всех известных загрязнителей, пропуская сквозь мембрану только молекулы кислорода и воды, защищая тем самым человеческий организм от влияния вредных веществ. Системы для воды, работающие по принципу обратного осмоса, делают воду не только вкусной, но и полезной, избавляя ее от примесей.
Решения BWT для обессоливания воды:
Преимуществ использования осмотической очистки очень много, вот только некоторые из них:
- вода идеально чистая, даже чище, нежели минеральная бутилированная.
- Благодаря встроенному минерализатору, вода насыщается полезными веществами — минералами.
- У вас под рукой будет неограниченное количество абсолютно чистой воды, которую можно использовать для любых целей — приготовления пищи, питья, купания, стирки.
- Отсутствие отложений на бытовых водонагревательных устройствах.
- Безопасная вода для детей.
Необходимость в чистой воде
Без воды невозможно существование ничего живого на Земле. В течение всей своей жизни человек употребляет до 75-ти тонн воды, «выпивая» при этом почти 90 процентов всех болезней, как утверждал знаменитый ученый Луи Пастер. Да и данные Всемирной организации здравоохранения также это подтверждают — ежегодно от употребления некачественной воды умирает более 25 миллионов человек на Земле. К тому же грязная вода почти на тридцать процентов ускоряет процесс старения. А в водопроводной воде, несмотря даже на наличие городских водоочистительных сооружений, содержатся десятки вредных химических соединений, а из них наиболее опасными считаются соли тяжелых металлов, растворенное железо, нитраты, пестициды, активный хлор и прочие.
Осмотические системы очистки воды
самые современные, эффективные, но в то же время и самые сложные устройства. Первоначально такие системы разрабатывались для очистки воды в космических кораблях и подводных лодках, в замкнутой системе. Но сейчас они широко применяются в промышленности и в быту — в промышленности их используют для обессоливания и опреснения морской воды, также для качественной очистки в химической, медицинской и пищевой промышленности — при производстве соков, бутилированной воды, алкогольной продукции.Технология очистки
В осмотической системе загрязненная вода вначале проходит через три фильтра механической очистки, после чего поступает на полупроницаемую мембрану, где происходит ее разделение на чистую и грязную воду, выводимую в дренаж или канализацию. В процессе очистки очищенная вода скапливается в специальной емкости, а уже оттуда через кран подается потребителям. По пути из емкости вода проходит сквозь фильтр финишной очистки и встроенный минерализатор, который обогащает ее полезными веществами ионами натрия, калия, магния кальция, что делает ее максимально полезной и повышает вкусовые качества.
Самый важный элемент осмотической системы очистки — полупроницаемая мембрана, диаметр которой составляет до 1-го Ангстрема (0,1 нанометра), что равняется размеру одной молекулы воды. В принципе, осмотическая система осуществляет водоочистку на атомарном уровне, поскольку через нее проходят только молекулы растворенного кислорода и воды. Ну а так как размер большинства веществ, содержащихся в воде больше 1-го Ангстрема, то они сквозь мембрану не проходят, остаются на ней. По мере загрязнения мембраны она промывается обратным током воды, после чего все это смывается в канализацию.
Благодаря такому барьеру из нее удаляются абсолютно все посторонние примеси, так что по своим свойствам очищенная вода близка к дистиллированной. Скептикам это дает повод утверждать, что после такой очистки вода становится вредной для здоровья, так как из нее вместе с вредными, удаляются и полезные элементы. А как известно, постоянное употребление дистиллированной воды не очень полезно для здоровья людей. Тем не менее, это не так, потому что минерализатор вновь насыщает воду полезными минералами. Поэтому можно с уверенностью говорить, что осмотическая система очистки воды — это лучшее, что придумано на данный момент.
Смотрите также:
Специфичность
Специфичность — высокая избирательность действия ферментов:
— реакционная/каталитическая специфичность (по отношению к катализируемой реакции) — фермент катализирует определенный тип каталитических превращенийодного или нескольких субстратов по одному из возможных путей,
—
субстратная специфичность (по отношению
к соответствующим субстратам) — способность
каждого фермента взаимодействовать
только с одним или несколькимиопределенными
субстратами
групповую (относительную),
стереоспецифичность,
редко двойственную специфичность.
Стереоспецифичность – катализ только одного из стереоизомеров, например:
специфичность к L- или D-аминокислотам – например, почти все ферменты человека взаимодействуют с L-аминокислотами,
ферменты метаболизма углеводов имеют специфичность к D-, а не кL-моносахаридам,
специфичность к цис- и транс-изомерам. Например, аспартаза реагирует только с транс-изомером – фумаровой кислотой, но не с малеатом (цис-изомер).
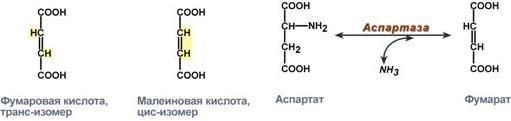
Стереоспецифичность аспартазы к транс-изомеру субстрата
Реакция расщепления мочевины |
3.Групповая специфичность– катализ субстратов с общими структурными особенностями, т.е. при наличии определенной связи или химической группы:
пепсин катализирует разрыв пептидной связи, образованной карбоксильными группами ароматических аминокислот (тромбин расщепляет пептидную связь только между аргинином и глицином).
например, наличие ОН-группы:алкогольдегидрогеназа окисляет до альдегидов одноатомные спирты (этанол, метанол, пропанол).
Гексокиназа катализирует присоединение фосфатной группы к ряду шестиуглеродных сахаров: глюкозе, маннозе, фруктозе, галактозе и др.
4. Двойственная специфичность – фермент взаимодействует с резко различающимися по структуре субстратами. Например, ксантиноксидаза окисляет не только гипоксантин и ксантин, но и альдегиды.
21. Клетка как осмотическая система. Осмос. Уравнение осматического давления.
Растительная клетка представляет собой осмотическую систему. Пектоцеллюлозная оболочка хорошо проницаема как для воды, так и для растворенных веществ. Однако плазмалемма и тонопласт обладают избирательной проницаемостью, легко пропускают воду и менее проницаемы, а в некоторых случаях непроницаемы для растворенных веществ. В этом можно убедиться, рассмотрев явления плазмолиза и тургора. Если поместить клетку в раствор более высокой концентрации, чем в клетке, то под микроскопом видно, что цитоплазма отстает от клеточной оболочки. Это особенно хорошо проявляется на клетке с окрашенным клеточным соком. Клеточный сок остается внутри вакуоли, а между цитоплазмой и оболочкой образуется пространство, заполненное внешним раствором. Явление отставания цитоплазмы от клеточной оболочки получило название плазмолиза. Плазмолиз происходит в результате того, что под влиянием более концентрированного внешнего раствора вода выходит из клетки (от своего большего химического потенциала к меньшему), тогда как растворенные вещества остаются в клетке. При помещении клеток в чистую воду или в слабо концентрированный раствор вода поступает в клетку. Количество воды в клетке увеличивается, объем вакуоли возрастает, клеточный сок давит на цитоплазму и прижимает ее к клеточной оболочке. Под влиянием внутреннего давления клеточная оболочка растягивается, в результате клетка переходит в напряженное состояние — тургор.
Наблюдения
за явлениями плазмолиза и тургора
позволяют изучить многие свойства
клетки. Явление плазмолиза показывает,
что клетка жива и цитоплазма сохранила
полупроницаемость. В мертвых клетках
мембрана не обладает полупроницаемостью,
не контролирует потоки веществ, и
осмотический выход воды не происходит.
По скорости и форме плазмолиза можно
судить о вязкости цитоплазмы. Наконец,
явление плазмолиза позволяет определить
величину осмотического потенциала
в клетке (плазмолитический метод). Этот
метод основан на подборе изоосмотического,
или изотонического, раствора, т. е.
имеющего осмотический потенциал (Ψ
Определение величины осмотического потенциала имеет большое значение, в частности для экологических исследований. Величина осмотического потенциала позволяет судить о максимальной способности растения поглощать воду из почвы и удерживать ее, несмотря на иссушающее действие атмосферы. Осмотический потенциал колеблется в широких пределах, от —5 до —200 бар. Осмотический потенциал около —1 бара наблюдается у водных растений. Осмотический потенциал, равный —200 бар, обнаружен у выжатого сока талофта Atriplex confertifolia. В 1 л сока этого растения содержится 67,33 г хлоридов. У большинства растений средней полосы осмотический потенциал колеблется от —5 до —30 бар. Вместе с тем необходимо отметить, что факторы, действующие на изменение осмотического потенциала, чрезвычайно разнообразны. Даже соседние, рядом расположенные клетки могут отличаться по величине осмотического потенциала. Обычно отрицательная величина осмотического потенциала больше у мелких клеток по сравнению с крупными. Установлены определенные градиенты осмотического потенциала в пределах одной ткани. Так, в тканях стебля отрицательный осмотический потенциал возрастает от периферии к центру и от основания к верхушке. В корне отрицательный осмотический потенциал, наоборот, постепенно снижается от основания к верхушке. В проводящих элементах стебля и корня, как правило, отрицательная величина осмотического потенциала очень низка (от —1 до —1,5 бара). В листьях осмотический потенциал колеблется от -10 до -18 бар. Осмотический потенциал различен у разных жизненных форм. У древесных Пород он более отрицателен, чем у кустарников, а у кустарников более отрицателен, чем у травянистых растении. Разные экологические группы различаются по величине осмотического потенциала. У растений пустынь осмотический потенциал более отрицателен, чем у степных растений; у степных более отрицателен, чем у луговых. Еще меньше осмотическая концентрация у растений болотных и водных местообитаний (соответственно наименее отрицательный осмотический потенциал). У светолюбивых растений осмотический потенциал более отрицательный, чем у теневыносливых. На величину осмотического потенциала влияет концентрация растворенных веществ в клеточном соке — это осмотически активные вещества (органические кислоты, соли, аминокислоты, сахара). Растение в определенной степени регулирует величину осмотического потенциала. Ферментативное превращение сложных нерастворимых веществ в растворимые (крахмала в сахара, белков в аминокислоты) приводит к возрастанию концентрации клеточного сока и повышению отрицательной величины осмотического потенциала. Увеличенное накопление растворимых солей также делает более отрицательным осмотический потенциал. Несмотря на то, что осмотический потенциал меняется в зависимости от внешних условий, все же для каждого вида эти изменения происходят в своих определенных пределах. Величину осмотического потенциала многие физиологи считают одной из характеристик данного вида растений.
Водный потенциал клетки.
Величина осмотического потенциала имеет большое значение для определения силы, которая вызывает поступление воды в клетку. Однако надо учесть, что клеточная оболочка, свободно пропуская воду и питательные вещества, обладает ограниченной растяжимостью. При поступлении в клетку воды, в ней развивается гидростатическое давление, которое заставляет плазмалемму прижиматься к клеточной оболочке. Клеточная оболочка растягивается и, в свою очередь, оказывает противодавление — это потенциал давления; он тем больше, чем больше поступает воды в клетку. Благодаря ограниченной растяжимости клеточной оболочки наступает такой момент, когда давление оболочки целиком уравновешивает силу осмотического поступления воды. С термодинамической точки зрения направление движения воды определяется величиной водного потенциала. Водный потенциал — это мера энергии, с которой вода поступает в клетку. Водный потенциал показывает, насколько активность воды в системе (клетке) меньше активности чистой воды. Водный потенциал чистой воды равен нулю. Присутствие растворимых веществ в водном растворе или в клетке уменьшает концентрацию воды, снижает ее активность. Когда на водный раствор действует давление (в случае клетки противодавление оболочки, или Ψдавл) молекулы воды сближаются друг с другом, и это приводит к увеличению энергии системы, к возрастанию активности воды.
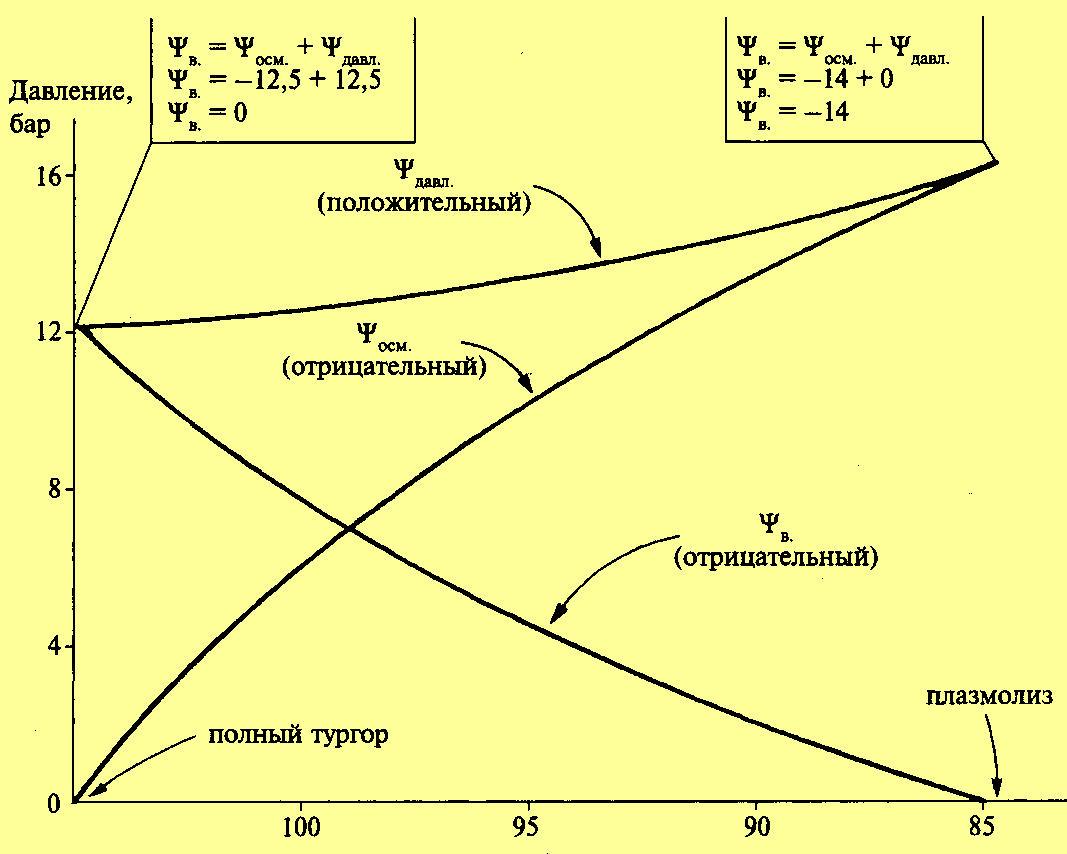
Относительное изменение объема клетки.
Таким образом водный потенциал клетки зависит прежде всего от концентрации осмотически действующих веществ — осмотического потенциала, который всегда отрицателен, и от потенциала давления в большинстве случаев положительного. Сказанное можно выразить следующим образом: Иначе говоря, водный потенциал показывает, насколько энергия воды в клетке меньше энергии чистой воды. В состоянии плазмолиза или завядания вода не давит на клеточную оболочку. Противодавление клеточной оболочки равно 0. Водный потенциал равен осмотическому потенциалу. По мере поступления воды в клетку появляется противодавление клеточной оболочки. В этом случае водный потенциал клетки будет равен разности между осмотическим потенциалом и противодавлением оболочки (потенциалом давления). Чем больше поступает воды в клетку, тем больше возрастает тургор и противодавление оболочки. Наконец наступает такой момент, при котором клеточная оболочка растягивается до предела, осмотический потенциал целиком уравновешивается противодавлением клеточной оболочки, а водный потенциал становится равным нулю. Из сказанного видно, что при переходе клетки из состояния плазмолиза к тургору водный потенциал меняется очень резко — от всей величины осмотического потенциала до нуля. Вместе с тем нельзя не отметить, что при наступлении полного тургора величина осмотического потенциала в результате поступления воды также несколько изменяется, он становится менее отрицательным. Однако это изменение составляет всего 15—20%. В обычных условиях осмотический потенциал клетки не уравновешен полностью противодавлением. Это показывает, что клеточная оболочка еще не полностью растянута и вода может поступать в клетку. Разница между осмотическим потенциалом клеточного сока и противодавлением клеточной оболочки определяет поступление воды в каждый данный момент. Вода всегда поступает в сторону более отрицательного водного потенциала: от той системы, где ее энергия больше, к той, где ее энергия меньше. Необходимо еще раз подчеркнуть, что именно водный потенциал определяет направление передвижения воды. Так, если рядом находятся две клетки А и Б, то вода будет поступать по градиенту не осмотического, а водного потенциала, в сторону более отрицательной величины последнего, т. е. из клетки А в клетку Б. Это будет происходить до того момента, пока водные потенциалы соседних клеток не выравняются. При завядании в клетках листа цитоплазма не отстает от клеточной стенки, как при плазмолизе, а сжимается и тянет ее за собой. При этом клеточная оболочка прогибается (циторриз). Развивается натяжение, или отрицательное давление, и потенциал давления приобретает отрицательное значение.
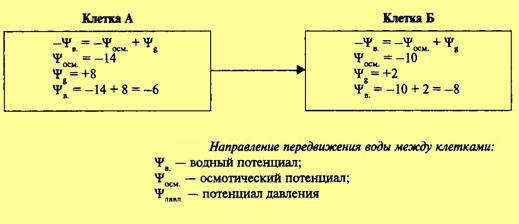
Таким образом, клетка проявляет себя как саморегулирующаяся система. Величина водного потенциала определяется степенью насыщенности клетки водой: чем меньше клетка насыщена водой, тем более отрицателен ее водный потенциал. Существует ряд методов, позволяющих определить. Наиболее простой метод заключается в том, что подбирается раствор, в котором размер клетки не меняется, а следовательно, вода не уходит из клетки и не поступает в нее. Зная молярную концентрацию раствора, можно рассчитать водный потенциал клетки. Говоря о поступлении воды в клетку, надо учитывать, что наряду с осмотическими силами в клетках существуют силы набухания. Набухание связано со способностью гидрофильных коллоидов притягивать к себе молекулы воды. Набухание может рассматриваться как особый вид диффузии, так как движение воды также идет по градиенту концентрации. Водный потенциал клеток становится более отрицательным благодаря присутствию органических веществ, связывающих воду. Силу набухания обозначают термином «матричный потенциал» ). Матричный потенциал определяется влиянием на поступление воды высокомолекулярных компонентов клетки: белков цитоплазмы, полисахаридов клеточной стенки, и особенно пектиновых веществ. Матричный потенциал всегда отрицателен. Хорошо известно, что если сухие семена положить в воду, то они будут увеличиваться в размере. Сила набухания у сухих семян достигает —1000 бар. Большое значение имеет не только для семян, но и для молодых меристематических клеток, в которых отсутствуют вакуоли и которые заполнены цитоплазмой. При поднятии воды на относительно большую высоту (например, у высоких деревьев) на величину давления оказывает влияние сила тяжести. В этом случае в уравнение водного потенциала вводят гравитационный потенциал Ψграв. Поскольку действие силы тяжести снижает активность воды, гравитационный потенциал всегда отрицателен. Возможным механизмом поступления воды является также электроосмос. Секреция воды является следствием разности электрических потенциалов, возникающих с наружной и внутренней стороны мембраны (тонопласта). При этом движение воды может быть вызвано накоплением катионов (К+, Na+), что в свою очередь происходит под влиянием разности электрических потенциалов. Может иметь значение также заглатывание воды клеткой в процессе пиноцетоза.
О́смос (от греч. ὄσμος — толчок, давление) — процесс односторонней диффузии через полупроницаемую мембрану молекул растворителя в сторону бо́льшей концентрации растворённого вещества из объёма с меньшей концентрацией растворенного вещества.
Более широкое толкование явления осмоса основано на применении Принципа Ле Шателье — Брауна: если на систему, находящуюся в устойчивом равновесии, воздействовать извне, изменяя какое-либо из условий равновесия (температура, давление, концентрация, внешнее электромагнитное поле), то в системе усиливаются процессы, направленные на компенсацию внешнего воздействия.
Явление осмоса наблюдается в тех средах, где подвижность растворителя больше подвижности растворённых веществ. Важным частным случаем осмоса является осмос черезполупроницаемую мембрану. Полупроницаемыми называют мембраны, которые имеют достаточно высокую проницаемость не для всех, а лишь для некоторых веществ, в частности, для растворителя. (Подвижность растворённых веществ в мембране стремится к нулю). Как правило, это связано с размерами и подвижностью молекул, например, молекула воды меньше большинства молекул растворённых веществ. Если такая мембрана разделяет раствор и чистый растворитель, то концентрация растворителя в растворе оказывается менее высокой, поскольку там часть его молекул замещена на молекулы растворённого вещества (см. Рис. 1). Вследствие этого, переходы частиц растворителя из отдела, содержащего чистый растворитель, в раствор будут происходить чаще, чем в противоположном направлении. Соответственно, объём раствора будет увеличиваться (а концентрация вещества уменьшаться), тогда как объём растворителя будет соответственно уменьшаться.
Например, к яичной скорлупе с внутренней стороны прилегает полупроницаемая мембрана: она пропускает молекулы воды и задерживает молекулы сахара. Если такой мембраной разделить растворы сахара с концентрацией 5 и 10 % соответственно, то через нее в обоих направлениях будут проходить только молекулы воды. В результате в более разбавленном растворе концентрация сахара повысится, а в более концентрированном, наоборот, понизится. Когда концентрация сахара в обоих растворах станет одинаковой, наступит равновесие. Растворы, достигшие равновесия, называются изотоническими. Если принять меры, чтобы концентрации не менялись, осмотическое давление достигнет постоянной величины, когда обратный поток молекул воды сравняется с прямым.
Осмос, направленный внутрь ограниченного объёма жидкости, называется эндосмосом, наружу — экзосмосом. Перенос растворителя через мембрану обусловлен осмотическим давлением. Это осмотическое давление возникает соответственно Принципу Ле Шателье из-за того, что система пытается выровнять концентрацию раствора в обеих средах, разделенных мембраной, и описывается вторым законом термодинамики. Оно равно избыточному внешнему давлению, которое следует приложить со стороны раствора, чтобы прекратить процесс, то есть создать условия осмотического равновесия. Превышение избыточного давления над осмотическим может привести к обращению осмоса — обратной диффузии растворителя.
В случаях, когда мембрана проницаема не только для растворителя, но и для некоторых растворённых веществ, перенос последних из раствора в растворитель позволяет осуществить диализ, применяемый как способ очистки полимеров иколлоидных систем от низкомолекулярных примесей, например электролитов.
Осмос играет важную роль во многих биологических процессах. Мембрана, окружающая нормальную клетку крови, проницаема лишь для молекул воды, кислорода, некоторых из растворённых в крови питательных веществ и продуктов клеточной жизнедеятельности; для больших белковых молекул, находящихся в растворённом состоянии внутри клетки, она непроницаема. Поэтому белки, столь важные для биологических процессов, остаются внутри клетки.
Осмос участвует в переносе питательных веществ в стволах высоких деревьев, где капиллярный перенос не способен выполнить эту функцию.
Осмос широко используют в лабораторной технике: при определении молярных характеристик полимеров, концентрировании растворов, исследовании разнообразных биологических структур. Осмотические явления иногда используются в промышленности, например при получении некоторых полимерных материалов, очистке высоко-минерализованной воды методом обратного осмоса жидкостей.
Клетки растений используют осмос также для увеличения объёма вакуоли, чтобы она распирала стенки клетки (тургорное давление). Клетки растений делают это путём запасания сахарозы. Увеличивая или уменьшая концентрацию сахарозы в цитоплазме, клетки могут регулировать осмос. За счёт этого повышается упругость растения в целом. С изменениями тургорного давления связаны многие движения растений (например, движения усов гороха и других лазающих растений). Пресноводныепростейшие также имеют вакуоль, но задача вакуолей простейших заключается лишь в откачивании лишней воды из цитоплазмы для поддержания постоянной концентрации растворённых в ней веществ.
Осмос также играет большую роль в экологии водоёмов. Если концентрация соли и других веществ в воде поднимется или упадёт, то обитатели этих вод погибнут из-за пагубного воздействия осмоса.
Первая в мире электростанция — прототип, использующая для выработки электричества явление осмоса, запущена компанией Statkraft 24 ноября 2009 года в Норвегии вблизи города Тофте. Солёная морская и пресная вода на электростанции разделенымембраной. Так как концентрация солей в морской воде выше, между солёной водой моря и пресной водой фьорда развивается явление осмоса — постоянный поток молекул воды через мембрану в сторону солёного раствора, в результате чего образуется давление пресной воды на мембрану.[1] Это давление соответствует давлению столба воды в 120 метров высотой, то есть достаточно высокому водопаду. Поток воды достаточен, чтобы приводить в действие гидротурбину, вырабатывающую энергию.[2] Производство носит ограниченный характер, основная цель — тестирование оборудования. Самый проблематичный компонент электростанции — мембраны. По оценкам специалистов Statkraft мировое производство может составить от 1 600 до 1 700 TWh, что сравнимо с потреблением Китая в 2002. Ограничение связано с принципом действия — подобные электростанции могут быть построены только на морском побережье.[3] Это не вечный двигатель, источником энергии является энергия солнца. Солнечное тепло отделяет воду от моря при испарении и посредством ветра переносит на сушу. Потенциальная энергия используется на гидроэлектростанциях, а химическая энергия долго оставалась без внимания.
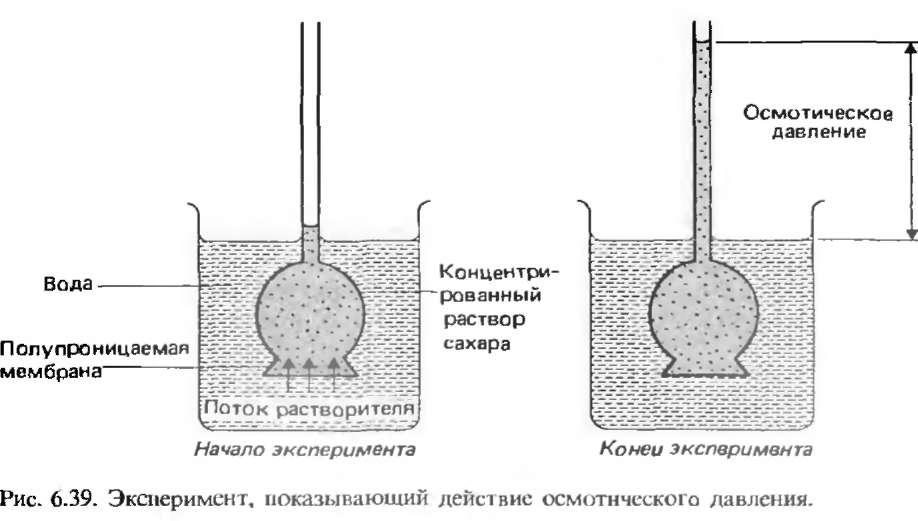
Осмос-это самопроизвольный переход растворителя через полупроницаемую мембрану из разбавленного раствора или чистого растворителя в концентрированный раствор. Это явление можно продемонстрировать с помощью прибора, схематически изображенного на рис. 6.39. Широкий конец трубки, закрытый мембраной животного происхождения (например, бычьим пузырем), наполняют раствором сахара и погружают в стакан с водой. Через некоторое время вода переходит сквозь мембрану в раствор сахара.
Мембрана, пропускающая частицы растворителя, но не пропускающая частицы растворенного вещества, называется полупроницаемой мембраной. Полупроницаемая мембрана пропускает частицы растворителя в обоих направлениях. Однако, поскольку с той стороны мембраны, где концентрация раствора выше, концентрация растворителя, наоборот, ниже, происходит результирующий переход растворителя в концентрированный раствор. Это приводит к установлению разности давлений по обе стороны мембраны. Давление, которое необходимо приложить к концентрированному раствору, чтобы воспрепятствовать переносу растворителя через мембрану, называется осмотическим давлением. Его обозначают греческой буквой п.
Осмотическое давление является коллигативным свойством, поскольку оно зависит только от концентрации растворенных частиц, а не от их химического состава.
Осмотическое давление играет важную роль в биологических процессах. Например, в организме животных некоторые типы клеток, например эритроциты, содержат солевой раствор. Эти клетки ограничены плазматической мембраной. В водной среде эритроциты подвергаются осмосу, набухают и лопаются. Однако, если они попадают в более концентрированный раствор соли, клетки сморщиваются.

Модули установки для получения сверхчистой воды на основе обратного осмоса. Такая вода необходима в полупроводниковой промышленности.
Амеба-одноклеточное существо. Вода непрерывно поступает в ее тело благодаря осмосу.
Растительные клетки содержат солевые растворы в особых полостях — вакуолях. Вакуоль окружена тонким слоем цитоплазмы, который обладает свойствами полупроницаемой мембраны и контролирует поглощение воды растительной клеткой.
Если давление, приложенное к концентрированному раствору, превышает осмотическое давление, растворитель переходит из концентрированного раствора через мембрану в разбавленный раствор. Этот процесс называется обратный осмос. Он находит промышленное применение с целью получения питьевой воды из морской воды.
Эксперименты, подобные описанному выше с сахарным раствором, показывают, что: 1) при постоянной температуре осмотическое давление прямо пропорционально разности концентраций в растворах, разделенных мембраной; 2) при фиксированной разности концентраций осмотическое давление прямо пропорционально абсолютной температуре.
Соотношение между осмотическим давлением и температурой аналогично уравнению состояния идеального газа (см. разд. 3.1). Оно называется уравнением Вант-Гоффа:
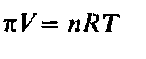 (11)
(11)
В этом уравнении тс — осмотическое давление, К-объем раствора, и-число молей растворенного вещества, T-абсолютная температура, Л-молярная газовая постоянная. Уравнение (11) может быть представлено в другой форме:
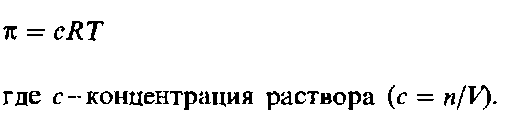
Уравнение Вант-Гоффа является приближенным и справедливо только для разбавленных растворов.
Определение относительной молекулярной массы растворенного вещества по осмотическому давлению раствора
Уравнение Вант-Гоффа может использоваться для определения относительной молекулярной массы растворенного вещества по создаваемому им осмотическому давлению, которое устанавливают экспериментальным путем. Этот метод особенно удобен для определения средней относительной молекулярной массы полимеров и других макро-молекулярных веществ.
8.Осмос и его законы.
Диффузия воды через полупроницаемую мембрану называется осмосом. Полупроницаемая мембрана – это мембрана, хорошо проницаемая для воды и непроницаемая или плохо проницаемая для растворенных в воде веществ. Осмотическая ячейка – это пространство, окруженное полупроницаемой мембраной и заполненное каким-либо водным раствором, способным развивать определенное осмотическое давление. Осмотическое давление (диффузное давление) – термодинамический параметр, характеризующий стремление раствора к понижению концентрации при соприкосновении с чистым растворителем вследствие встречной диффузии молекул растворённого вещества и растворителя. Если раствор отделен от чистого растворителя полупроницаемой мембраной, то возможна лишь односторонняя диффузия – осмотическое всасывание растворителя через мембрану в раствор. В этом случае осмотическое давление становится доступной для прямого измерения величиной. Оно равно избыточному давлению, приложенному со стороны раствора при осмотическом равновесии. Осмотическое давление обусловлено понижением химического потенциала растворителя в присутствии растворённого вещества. Тенденция системы выравнивать химические потенциалы во всех частях своего объёма и переходить в состояние с более низким уровнем свободной энергии вызывает осмотический (диффузионный) перенос вещества. Осмотическое давление в идеальных и предельно разбавленных растворах не зависит от природы растворителя и растворённых веществ; при постоянной температуре оно определяется только числом «кинетических элементов» (ионов, молекул, ассоциатов или коллоидных частиц) в единице объёма раствора. Осмотическое давление (Р) численно равно давлению, которое оказало бы растворённое вещество, если бы оно при данной температуре находилось в состоянии идеального газа и занимало объём, равный объёму раствора. Осмотическое давление измеряют с помощью специальных приборов (осмометров), определяя избыточное гидростатическое давление столба жидкости в трубке осмометра после установления осмотического равновесия. Осмос является основным механизмом поступления воды в растительную клетку. Все клеточные мембраны, в том числе плазмалемма и тонопласт, являются полупроницаемыми мембранами. Вода проходит в клетку через водные поры в плазмалемме, образованные специальными белками – аквапоринами.Благодаря осмотическому притоку воды в клетку там возникает гидростатическое давление, называемое тургорным. Это давление прижимает цитоплазму к клеточной стенке и растягивает ее. Клеточная стенка имеет ограниченную эластичность и оказывает равное противодавление. Эластическое растяжение ткани благодаря тургорному давлению ее клеток придает твердость неодревесневшим частям растений. Завядающие побеги становятся дряблыми, так как при потере воды тургорное давление падает. Тургорное давление противодействует притоку воды в клетку. Давление, с которым вода осмотически притекает в клетку, равно, таким образом, разности осмотического давления π и тургорного давления P. Эту величину называют сосущей силой S:
S = π – P.
Вода поступает в клетку из внешнего раствора, если его потенциальное осмотическое давление меньше сосущей силы клетки, и, наоборот, вода выходит из клетки в раствор с более высоким потенциальным осмотическим давлением.
Осмос живой клетки | Русфильтр
Осмосом называют прохождение воды через избирательно проницаемую мембрану, в частности через клеточную мембрану. В случае клеточной мембраны осмос частично обусловлен диффузией отдельных молекул воды сквозь эту мембрану, а частично — током воды через особые поры в мембране. Поскольку концентрация всякого водного раствора зависит от количества растворенного в воде вещества, вода стремится переходить из более разбавленного раствора (где концентрация воды выше) в более концентрированный (где концентрация воды соответственно ниже).
Осмотическое движение воды зависит от двух главных факторов:
- от общей концентрации всех растворенных в воде частиц по обе стороны мембраны и
- от давления, создаваемого каждым раствором.
При прочих равных условиях вода стремится переходить через избирательно проницаемую мембрану от менее концентрированного раствора к раствору с более высокой общей концентрацией всех растворенных частиц (рис.1. ).
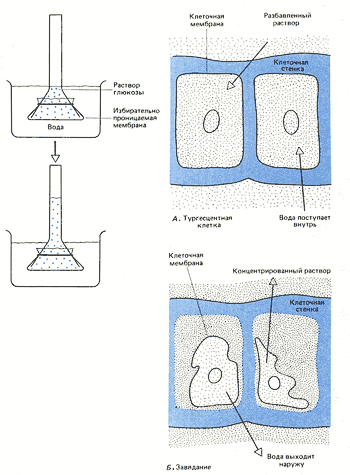
Рис. 1. Осмос в искусственной системе. Трубку, содержащую раствор глюкозы и закрытую с одного конца мембраной, пропускающей воду, но не пропускающей глюкозу, опускают закрытым концом в сосуд с водой. Вода может проходить через мембрану в том и в другом направлении; однако молекулы глюкозы в трубке мешают движению соседних молекул воды, и потому больше воды входит в трубку, чем выходит из нее. Раствор поднимается в трубке до тех пор, пока давление его столба не станет достаточным для того, чтобы вытеснять воду из трубки с такой же скоростью, с какой она поступает внутрь.
Однако при этом в какой-то момент вода, поступившая в более концентрированный раствор, может развить такое давление, что это давление будет вытеснять ее наружу с такой же скоростью, с какой она поступает внутрь.
Не обладая способностью насасывать или откачивать воду непосредственно, клетки регулируют приток и отток воды, изменяя концентрацию находящихся в них растворенных веществ. Чтобы поглотить больше воды, клетка поглощает больше ионов различных солей, молекул глюкозы или других растворимых соединений. В результате в клетке повышается концентрация растворенных частиц. Вода по законам осмоса начинает поступать в клетку, стремясь к выравниванию своей собственной концентрации по обе стороны мембраны.
Так работает эта система до тех пор, пока концентрация растворенных веществ вне клетки и в клетке примерно одинакова. А что происходит, когда концентрация внутри и вне клетки очень сильно разнится? Если в среде концентрация растворенных веществ выше, чем в самой клетке, или если средой для клетки служит практически сухой воздух, то клетка теряет воду и сморщивается, как это бывает, когда растения привядают в сухой жаркий день. С оттоком воды содержимое клетки сжимается и отходит от клеточных стенок (рис. 2).
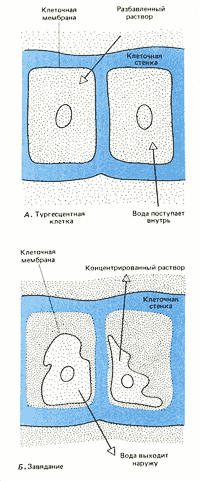
Рис. 2. Тургор и завядание у растений.
А. Растительные клетки, окруженные разбавленным раствором, поглощают воду путем осмоса через клеточную мембрану и остаются тургесцентными.
Б. Растительные клетки, окруженные концентрированным раствором, теряют воду вследствие осмоса, и растение завядает.
Если, однако, увядшее растение поместить в воду, то вода вновь поступает в клетки. Они становятся тургесцентными, т.е. набухают от воды и снова прижимаются к клеточным стенкам, подчиняясь тургорному давлению, направленному изнутри наружу. Клеточные стенки способны растягиваться лишь до известного предела, после которого они начинают оказывать противодавление, вытесняющее воду из клеток с такой же скоростью, с какой она в них поступает. Таким способом клеточные стенки защищают клетки: не дают им лопнуть под напором избытка воды.
Многие животные клетки, если поместить их в чистую воду или в очень разбавленный раствор, лопаются, потому что у них нет клеточных стенок (рис. 3).
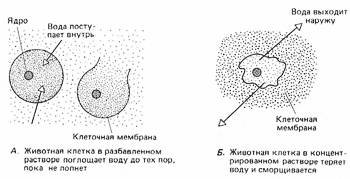
А. Животная клетка в разбавленном растворе поглощает воду до тех пор, пока не лопнет
Б. Животная клетка в концентрированном растворе теряет воду и сморщивается
Во избежание этого лекарственные препараты, предназначенные для внутривенного введения, готовят не на чистой воде, а на специальных солевых растворах. Животные клетки, соприкасающиеся с водой постоянно, например клетки, выстилающие желудочно-кишечный тракт человека, обладают приспособлениями, которые не дают им поглощать слишком много воды. Когда мы пьем воду, она всасывается и распределяется постепенно; именно поэтому клетки в нашем организме и не лопаются.
Явление осмоса — Libtime
- Главная
- Агрономия
- Явление осмоса
Осмометр Дютроше
Явление осмоса можно наблюдать в осмометре. Осмометр Дютроше состоит из стеклянной трубки, на расширенный конец которой натянут животный пузырь или пергамент. В трубку наливают концентрированный раствор сахара и погружают ее в воду или слабый раствор того же сахара. Вода будет поступать в трубку через пузырь, так как концентрация ее там меньше; в результате объем раствора в осмометре увеличится, и раствор поднимется по трубке. Осмометр Дютроше. Для того чтобы задержать проникновение воды в осмометр, надо приложить к раствору давление, которое уравновесит давление диффузии воды. Чем больше концентрация раствора в осмометре, тем выше будет подниматься столб жидкости в трубке и тем большее давление надо приложить, чтобы остановить поступление воды в осмометр. Высота раствора в трубке служит, таким образом, показателем концентрации раствора, вызывающего осмотическое давление.Осмотическое давление
Осмотическое давление — своеобразное явление. Оно возникает только в том случае, если раствор отделен от растворителя (или раствора меньшей концентрации) полупроницаемой перепонкой. Если же раствор находится, например, в стеклянном сосуде, то никаких признаков осмотического давления стенки сосуда не испытывают. Величина осмотического давления пропорциональна количеству частиц растворенного вещества (молекул и ионов) и температуре. Чем выше концентрация раствора, тем больше будет его осмотическое давление, ибо число молекул растворенного вещества будет больше. При одной и той же молярной концентрации растворов неэлектролита и электролита осмотическое давление второго раствора будет выше, так как часть его молекул диссоциируют на ионы и суммарное число частиц в нем будет больше. Если раствор отделен полупроницаемой перепонкой от чистой воды, то вода проникает в раствор со всей возможной скоростью, зависящей от концентрации раствора и других уже упомянутых условий. Наибольшую возможную для данного раствора величину осмотического давления называют осмотическим потенциалом. Величину осмотического потенциала и осмотического давления выражают в атмосферах.Растительная клетка — осмотическая система
Растительная клетка представляет собой осмотическую систему; протоплазма играет роль полупроницаемой перепонки, так как она пропускает воду и задерживает растворенные в воде вещества, а клеточный сок — осмотически деятельного раствора. Его концентрацией обусловливается величина осмотического потенциала. В полупроницаемости протоплазмы можно убедиться при помощи плазмолиза. Плазмолиз — это отставание протоплазмы от оболочки в результате диффундирования воды из вакуоли в более концентрированный наружный раствор. Плазмолиз получают, помещая растительную клетку в безвредный для нее раствор, концентрация которого больше концентрации клеточного сока. Наружный раствор отсасывает воду из клеточного сока через полупроницаемую протоплазму, объем его уменьшается, протоплазма следует за клеточным соком и отстает от клеточной оболочки, проницаемой как для воды, так и для растворенных веществ.Тургорное давление
При помещении растительной клетки в воду последняя проходит через клеточную оболочку, плазмалемму и тонопласт и попадает в вакуолю. Объем клеточного сока увеличивается, протоплазма отодвигается к оболочке, оказывая на нее давление. Чем больше воды поступит в клеточный сок, тем больше будет его объем и тем сильнее давление клеточного сока на протоплазму, а через нее и на оболочку. Давление протоплазмы на оболочку клетки называется тургорным давлением.Тургорное натяжение
Под влиянием внутреннего давления клеточная оболочка переходит в напряженное состояние, которое называется тургором, или тургорным натяжением. Тургорное натяжение равно тургорному давлению, но направлены они в разные стороны: тургорное натяжение к центру клетки, тургорное давление к периферии.Соленый киловатт: осмос | Журнал Популярная Механика
В один прекрасный день 1747 года французский аббат Нолле слил недопитый намедни бордо в свиной мочевой пузырь, доставленный с кухни, и погрузил его в бочонок с водой. Через 262 года, 24 ноября 2009-го, норвежская кронпринцесса Метте-Марит пригубила бокал с шампанским. Как же связаны эти два события? И Нолле, и принцесса совершили выдающиеся открытия. Аббат первым в мире сумел описать феномен осмоса и базовые свойства мембраны, а Метте-Марит, разрезав символическую ленточку, открыла первую в мире осмотическую электростанцию Statcraft в Тофте.
О том, чем на самом деле наполнил вошедший в историю свиной пузырь аббат, а по совместительству великий физик-экспериментатор Жан-Антуан Нолле, можно дискутировать. Но наличие воды в обоих сосудах (пузыре и бочке) неоспоримо. Разница состоит лишь в концентрации растворенного в ней спирта. Именно эта разница дала толчок диффузии воды через полупроницаемую мембрану из бочонка в пузырь. По тому, как раздулся пузырь, можно было понять, что явление это рождает весьма значительную однонаправленную силу, которую Нолле назвал осмотическим давлением. А осмос он определил как процесс диффузии растворителя из менее концентрированного раствора в более концентрированный.
В наши дни норвежская компания Statcraft, лидер европейского рынка экологически чистой энергетики, нашла способ превратить это давление в электричество. Новая технология — единственная, способная извлекать джоули из естественной разницы содержания минеральных солей в пресной и морской воде, а не из кинетической энергии их движения. По оценкам норвежцев, мировые ресурсы возобновляемой осмотической энергии составляют от 1,6 до 1,7 тераватт — примерно столько же в 2004 году потребовалось миллиардному Китаю! В отличие от капризного ветра, прибоя и солнца, процессы осмоса не останавливаются ни на секунду 24 часа в сутки круглый год.
 Для работы осмотической электростанции не требуются специальные инженерные сооружения: печи, реакторы, плотины, градирни. Первая в мире электростанция на осмосе расположилась в пустующем складе деревоперерабатывающего завода.
Для работы осмотической электростанции не требуются специальные инженерные сооружения: печи, реакторы, плотины, градирни. Первая в мире электростанция на осмосе расположилась в пустующем складе деревоперерабатывающего завода.
Выпить море
Вообще-то явление осмоса используется в промышленных масштабах уже более 40 лет. Только это не классический прямой осмос аббата Нолле, а так называемый обратный осмос — искусственный процесс проникновения растворителя из концентрированного в разбавленный раствор под действием давления, превышающего естественное осмотическое давление. Такая технология применяется в опреснительных и очистительных установках с начала 1970-х. Соленая морская вода нагнетается на специальную мембрану и, проходя через ее поры, лишается значительной доли минеральных солей, а заодно бактерий и даже вирусов. Для прокачивания соленой или загрязненной воды приходится затрачивать большие объемы энергии, но игра стоит свеч — на планете существует множество регионов, где дефицит питьевой воды является острейшей проблемой.
Теоретические разработки в этой области появились еще в начале ХХ века, но для их реализации не хватало главного — подходящей осмотической мембраны. Такая мембрана должна была выдерживать давление, в 20 раз превышающее давление обычного бытового водопровода, и иметь чрезвычайно высокую пористость. Создание материалов с подобными свойствами стало возможным после Второй мировой, когда накопленный в ходе военных проектов научный потенциал дал толчок развитию технологий производства синтетических полимеров.

 Принципиальная схема Трудно поверить, что одна лишь разница в концентрации двух растворов способна создать серьезную силу, однако это действительно так: осмотическое давление может поднять уровень морской воды на 120 м.
Принципиальная схема Трудно поверить, что одна лишь разница в концентрации двух растворов способна создать серьезную силу, однако это действительно так: осмотическое давление может поднять уровень морской воды на 120 м.
Наиболее значительный прорыв в этой области произошел в 1959 году. Сидней Лоэб и Шриниваса Суранджан из Калифорнийского университета в Лос-Анджелесе разработали спиральную анизотропную мембрану, способную выдерживать колоссальное давление, эффективно задерживать минеральные соли и механические частицы размером до 5 мкм и главное — обладающую высокой пропускной способностью при минимальных размерах. Изобретение Лоэба и Суранджана сделало осмотическое опреснение экономически выгодным бизнесом. В начале 1960-х в калифорнийской Коалинге Лоэб построил первую в мире опреснительную станцию на эффекте PRO (Pressure retarded osmosis), а затем перебрался в Израиль, где на средства ЮНЕСКО продолжил свои исследования. При участии Лоэба в 1967 году в местечке Йотвата была построена опреснительная установка мощностью 150 м³ в сутки, производившая чистую питьевую воду из подземного озера с соленостью, десятикратно превышавшей морскую. Еще через три года технология PRO была защищена американским патентом.
Осмос и космос

Мембранная лаборатория в Центре NASA им. Эймса уже много лет подряд занимается решением проблемы обеспечения обитателей космических станций питьевой водой. Ученые разработали технологию DOC, комбинирующую два разнонаправленных процесса — прямой и обратный осмос. При обратном осмосе мембрана работает как фильтр тонкой очистки и требует больших затрат энергии. Прямой осмос, наоборот, производит ее. Каждый из этих процессов по отдельности лишает водные растворы подавляющего количества примесей. В результате получается так называемая серая вода, которую можно использовать для гигиенических целей. Для того чтобы сделать из серой воды питьевую, раствор проходит этап мембранной очистки без дополнительного нагревания и далее очистку от бактерий и вирусов в подсистеме каталитического окисления. Балансовая энергоемкость DOC достаточно низка для применения в космосе.
Оригинальный способ очистки воды для космических станций представила американская компания Osmotek. Для сбора продуктов жизнедеятельности она предлагает использовать мембранные пакеты наподобие чайных с содержащимся в них активированным углем. Мембрана пропускает наружу лишь воду с незначительным количеством загрязнений. Этот первичный раствор затем попадает в мембранную камеру со специальным концентрированным субстратом в другой части. Возникающее явление прямого осмоса завершает процесс.
Компания Oasys обещает снизить расход энергии осмотических опреснительных установок ни много ни мало в десять раз. Правда, в данном случае речь идет не об обратном, а о прямом осмосе. И не простом, а модифицированном. Его суть заключается в наличии на ответной стороне обычной PRO-мембраны патентованного вытягивающего раствора с высоким содержанием аммиака, двуокиси углерода и других химикатов. При контакте двух растворов возникает явление осмоса и происходит очищение исходного сырья от примесей. Изюминка методики Oasys в том, что поток чистой пресной воды не смешивается с вытягивающим раствором.
Опыты по превращению осмотического давления в электрическую энергию с использованием мембран Лоэба-Суранджана проводились различными научными группами и компаниями с начала 1970-х. Принципиальная схема этого процесса была очевидной: поток пресной (речной) воды, проникающий сквозь поры мембраны, наращивает давление в резервуаре с морской водой, тем самым позволяя раскручивать турбину. Затем отработанная солоноватая вода выбрасывается в море. Проблема была лишь в том, что классические мембраны для PRO были слишком дороги, капризны и не обеспечивали необходимой мощности потока. С мертвой точки дело сдвинулось в конце 1980-х, когда за решение задачи взялись норвежские химики Торлейф Хольт и Тор Торсен из института SINTEF.

Космический размах
Мембраны Лоэба требовали клинической чистоты для поддержания максимальной производительности. Конструкция мембранного модуля опреснительной станции предусматривала обязательное наличие первичного фильтра грубой очистки и мощного насоса, сбивавшего мусор с рабочей поверхности мембраны.
Хольт и Торсен, проанализировав характеристики большинства перспективных материалов, остановили свой выбор на недорогом модифицированном полиэтилене. Их публикации в научных журналах привлекли внимание специалистов из Statcraft, и норвежских химиков пригласили продолжить работу под покровительством энергетической компании. В 2001 году мембранная программа Statcraft получила государственный грант. На полученные средства была построена экспериментальная осмотическая установка в Сунндальсьоре для тестирования образцов мембран и обкатки технологии в целом. Площадь активной поверхности в ней была чуть выше 200 м².
 Не стенка, а обои На схематичных изображениях осмотическую мембрану рисуют в виде стенки. На самом деле она представляет собой рулон, заключенный в цилиндрический корпус. В его многослойной структуре чередуются слои пресной и соленой воды. Поперечный разрез демонстрирует, как организованы
потоки воды внутри осмотического цилиндра. Чем больше
таких модулей установят на станции, тем больше энергии
она сможет вырабатывать.
Не стенка, а обои На схематичных изображениях осмотическую мембрану рисуют в виде стенки. На самом деле она представляет собой рулон, заключенный в цилиндрический корпус. В его многослойной структуре чередуются слои пресной и соленой воды. Поперечный разрез демонстрирует, как организованы
потоки воды внутри осмотического цилиндра. Чем больше
таких модулей установят на станции, тем больше энергии
она сможет вырабатывать.
Для ускорения процесса в команду были приглашены инженеры из специализированной мембранной лаборатории NASA. Дело в том, что еще со времен подготовки к лунной программе Apollo при Центре NASA им. Эймса проводились глубокие исследования технологий опреснения и очистки водных растворов. Опыт американцев пришелся как нельзя кстати, и к 2008 году у Statcraft появились первые образцы спиральных полиимидных мебран для будущих осмотических электростанций. Их производительность составила 1 Вт на 1 м² при диффузии 10 л пресной воды в секунду под давлением 10 бар.
На станции в Тофте работают именно такие мембранные модули общей площадью 2000 м². Для выработки 4кВт этого вполне достаточно, но для полноценной 25-мегаваттной станции потребовалось бы аж 5 млн квадратов. Разумеется, мембраны для осмотических электростанций должны быть гораздо эффективнее нынешних. Стайн Эрик Скиллхаген, вице-президент Statcraft, курирующий программу, утверждает, что сейчас компания тестирует спиральные образцы из полых волокон производительностью 3 Вт/м2, а к 2015 году появятся плоские 5-ваттные мембраны. Кроме того, норвежцы внимательно изучают сторонние разработки в этой области и активно сотрудничают со специалистами из General Electric, Hydranautics, Dow и японской Toray.
 Голландская батарейка В Голландии каждую секунду в соленое море низвергается 3300 кубометров речной воды. Ученые подсчитали, что ее суммарный энергетический потенциал составляет 4,5*109 Вт. Исследователи из KEMA также намерены выловить хотя бы часть энергии из этой бездонной бочки, но без лишней, по их мнению, механики. И такая возможность существует. Пока — в виде экспериментальной установки обратного электродиализа RED (reverse electrodialysis). В ней также используются морская и пресная вода, разделенные полупроницаемыми границами. Вот только мембран здесь две, и они выполняют роль электродов. Ведь RED — это батарея, работающая благодаря разнице в концентрациях ионов в двух средах. Эта разница и создает слабое напряжение на поверхности анодной и катодной мембран. Если из них собрать пакет, то вольтаж получится весьма ощутимым. Например, батарейка размером со стандартный морской контейнер выдает почти 250 кВт. KEMA с 2006 года эксплуатирует маленькую 50-киловаттную установку в Харлингене. На ней тестируются способы очистки и предотвращения загрязнения мембран биоматериалом. Клиническая чистота — критически важный фактор эффективной работы системы.
Голландская батарейка В Голландии каждую секунду в соленое море низвергается 3300 кубометров речной воды. Ученые подсчитали, что ее суммарный энергетический потенциал составляет 4,5*109 Вт. Исследователи из KEMA также намерены выловить хотя бы часть энергии из этой бездонной бочки, но без лишней, по их мнению, механики. И такая возможность существует. Пока — в виде экспериментальной установки обратного электродиализа RED (reverse electrodialysis). В ней также используются морская и пресная вода, разделенные полупроницаемыми границами. Вот только мембран здесь две, и они выполняют роль электродов. Ведь RED — это батарея, работающая благодаря разнице в концентрациях ионов в двух средах. Эта разница и создает слабое напряжение на поверхности анодной и катодной мембран. Если из них собрать пакет, то вольтаж получится весьма ощутимым. Например, батарейка размером со стандартный морской контейнер выдает почти 250 кВт. KEMA с 2006 года эксплуатирует маленькую 50-киловаттную установку в Харлингене. На ней тестируются способы очистки и предотвращения загрязнения мембран биоматериалом. Клиническая чистота — критически важный фактор эффективной работы системы.
Кстати, мембрана для прямого осмоса — это не тонкая стенка, которую рисуют на упрощенных схемах, а длинный рулон, заключенный в цилиндрический корпус. Соединения с корпусом сделаны таким образом, что во всех слоях рулона с одной стороны мембраны всегда находится пресная вода, а с другой- морская.
Энергия глубин
Разница между соленостью (по-научному — градиент солености) пресной и морской воды — базовый принцип работы осмотической электростанции. Чем она больше, тем выше объем и скорость потока на мембране, а следовательно, и количество энергии, вырабатываемой гидротурбиной. В Тофте пресная вода самотеком поступает на мембрану, в результате осмоса давление морской воды по ту сторону резко возрастает. Силища у осмоса колоссальная — давление может поднять уровень морской воды на 120 м.

Далее полученная разбавленная морская вода устремляется через распределитель давления на лопатки турбины и, отдав им всю свою энергию, выбрасывается в море. Распределитель давления отбирает часть энергии потока, раскручивая насосы, закачивающие морскую воду. Таким образом удается значительно повысить эффективность работы станции. По оценке Рика Стовера, главного технолога компании Energy Recovery, производящей такие устройства для опреснительных заводов, КПД передачи энергии в распределителях приближается к 98%. Точно такие же аппараты при опреснении помогают доставлять питьевую воду в жилые дома.
Как замечает Скиллхаген, в идеале осмотические электростанции нужно совмещать с опреснительными установками — соленость остаточной морской воды в последних в 10 раз выше естественного уровня. В таком тандеме эффективность выработки энергии возрастет не менее чем вдвое.
Строительные работы в Тофте начались осенью 2008 года. На территории завода по производству целлюлозы компании Sódra Cell был арендован пустующий склад. На первом этаже устроили каскад сетчатых и кварцевых фильтров для очистки речной и морской воды, а на втором — машинный зал. В декабре того же года был осуществлен подъем и монтаж мембранных модулей и распределителя давления. В феврале 2009-го группа водолазов проложила по дну залива два параллельных трубопровода — для пресной и морской воды.

Забор морской воды осуществляется в Тофте с глубин от 35 до 50 м — в этом слое ее соленость оптимальна. Кроме того, там она значительно чище, чем у поверхности. Но, несмотря на это, мембраны станции требуют регулярной чистки от забивающих микропоры органических остатков.
С апреля 2009 года электростанция эксплуатировалась в пробном режиме, а в ноябре, с легкой руки принцессы Метте-Марит, была запущена на всю катушку. Скиллхаген уверяет, что вслед за Тофте у Statcraft появятся и другие аналогичные, но более совершенные проекты. И не только в Норвегии. По его словам, подземный комплекс размером с футбольное поле способен бесперебойно снабжать электричеством целый город с 15 000 индивидуальных домов. Причем, в отличие от ветряков, такая осмотическая установка практически бесшумна, не изменяет привычный ландшафт и не влияет на здоровье человека. А о пополнении запасов соленой и пресной воды в ней позаботится сама природа.
Статья опубликована в журнале «Популярная механика» (№1, Январь 2011).Осмос — это… Что такое Осмос?
О́смос (от греч. ὄσμος — толчок, давление) — процесс односторонней диффузии через полупроницаемую мембрану молекул растворителя в сторону бо́льшей концентрации растворённого вещества (меньшей концентрации растворителя).
Более широкое толкование явления осмоса основано на применении Принципа Ле Шателье — Брауна: если на систему, находящуюся в устойчивом равновесии, воздействовать извне, изменяя какое-либо из условий равновесия (температура, давление, концентрация, внешнее электромагнитное поле), то в системе усиливаются процессы, направленные на компенсацию внешнего воздействия.
 Жан-Антуан Нолле
Жан-Антуан НоллеИстория
Впервые осмос наблюдал А. Нолле в 1748, однако исследование этого явления было начато спустя столетие.
Суть процесса
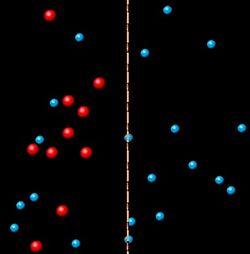 Рис. 1. Осмос через полупроницаемую мембрану. Частицы растворителя (синие) способны пересекать мембрану, частицы растворённого вещества (красные) — нет.
Рис. 1. Осмос через полупроницаемую мембрану. Частицы растворителя (синие) способны пересекать мембрану, частицы растворённого вещества (красные) — нет.Явление осмоса наблюдается в тех средах, где подвижность растворителя больше подвижности растворённых веществ. Важным частным случаем осмоса является осмос через полупроницаемую мембрану. Полупроницаемыми называют мембраны, которые имеют достаточно высокую проницаемость не для всех, а лишь для некоторых веществ, в частности, для растворителя. (Подвижность растворённых веществ в мембране стремится к нулю). Как правило, это связано с размерами и подвижностью молекул, например, молекула воды меньше большинства молекул растворённых веществ. Если такая мембрана разделяет раствор и чистый растворитель, то концентрация растворителя в растворе оказывается менее высокой, поскольку там часть его молекул замещена на молекулы растворённого вещества (см. Рис. 1). Вследствие этого, переходы частиц растворителя из отдела, содержащего чистый растворитель, в раствор будут происходить чаще, чем в противоположном направлении. Соответственно, объём раствора будет увеличиваться (а концентрация вещества уменьшаться), тогда как объём растворителя будет соответственно уменьшаться.
Например, к яичной скорлупе с внутренней стороны прилегает полупроницаемая мембрана: она пропускает молекулы воды и задерживает молекулы сахара. Если такой мембраной разделить растворы сахара с концентрацией 5 и 10 % соответственно, то через нее в обоих направлениях будут проходить только молекулы воды. В результате в более разбавленном растворе концентрация сахара повысится, а в более концентрированном, наоборот, понизится. Когда концентрация сахара в обоих растворах станет одинаковой, наступит равновесие. Растворы, достигшие равновесия, называются изотоническими. Если принять меры, чтобы концентрации не менялись, осмотическое давление достигнет постоянной величины, когда обратный поток молекул воды сравняется с прямым.
Осмос, направленный внутрь ограниченного объёма жидкости, называется эндосмосом, наружу — экзосмосом. Перенос растворителя через мембрану обусловлен осмотическим давлением. Это осмотическое давление возникает соответственно Принципу Ле Шателье из-за того, что система пытается выравнять концентрацию раствора в обоих средах, разделенных мембраной, и описывается вторым законом термодинамики. Оно равно избыточному внешнему давлению, которое следует приложить со стороны раствора, чтобы прекратить процесс, то есть создать условия осмотического равновесия. Превышение избыточного давления над осмотическим может привести к обращению осмоса — обратной диффузии растворителя.
В случаях, когда мембрана проницаема не только для растворителя, но и для некоторых растворённых веществ, перенос последних из раствора в растворитель позволяет осуществить диализ, применяемый как способ очистки полимеров и коллоидных систем от низкомолекулярных примесей, например электролитов.
Значение осмоса
Осмос играет важную роль во многих биологических процессах. Мембрана, окружающая нормальную клетку крови, проницаема лишь для молекул воды, кислорода, некоторых из растворённых в крови питательных веществ и продуктов клеточной жизнедеятельности; для больших белковых молекул, находящихся в растворённом состоянии внутри клетки, она непроницаема. Поэтому белки, столь важные для биологических процессов, остаются внутри клетки.
Осмос участвует в переносе питательных веществ в стволах высоких деревьев, где капиллярный перенос не способен выполнить эту функцию.
Осмос широко используют в лабораторной технике: при определении молярных характеристик полимеров, концентрировании растворов, исследовании разнообразных биологических структур. Осмотические явления иногда используются в промышленности, например при получении некоторых полимерных материалов, очистке высоко-минерализованной воды методом обратного осмоса жидкостей.
Клетки растений используют осмос также для увеличения объёма вакуоли, чтобы она распирала стенки клетки (тургорное давление). Клетки растений делают это путём запасания сахарозы. Увеличивая или уменьшая концентрацию сахарозы в цитоплазме, клетки могут регулировать осмос. За счёт этого повышается упругость растения в целом. С изменениями тургорного давления связаны многие движения растений (например, движения усов гороха и других лазающих растений). Пресноводные простейшие также имеют вакуоль, но задача вакуолей простейших заключается лишь в откачивании лишней воды из цитоплазмы для поддержания постоянной концентрации растворённых в ней веществ.
Осмос также играет большую роль в экологии водоёмов. Если концентрация соли и других веществ в воде поднимется или упадёт, то обитатели этих вод погибнут из-за пагубного воздействия осмоса.
Использование в промышленности
Первая в мире электростанция — прототип, использующая для выработки электричества явление осмоса, запущена компанией Statkraft 24 ноября 2009 года в Норвегии вблизи города Тофте. Солёная морская и пресная вода на электростанции разделены мембраной; так как концентрация солей в морской воде выше, между солёной водой моря и пресной водой фьорда развивается явление осмоса, — постоянный поток молекул воды через мембрану в сторону солёной воды. В результате чего давление солёной воды возрастает.[1] Это давление соответствует давлению столба воды в 120 метров высотой, то есть достаточно высокому водопаду. Поток воды достаточен, чтобы приводить в действие гидротурбину, вырабатывающую энергию.[2] Производство носит ограниченный характер, основная цель — тестирование оборудования. Самый проблематичный компонент электростанции — мембраны. По оценкам специалистов Statkraft мировое производство может составить от 1 600 до 1 700 TWh, что сравнимо с потреблением Китая в 2002. Ограничение связано с принципом действия — подобные электростанции могут быть построены только на морском побережье.[3] Это не вечный двигатель, источником энергии является энергия солнца. Солнечное тепло отделяет воду от моря при испарении и посредством ветра переносит на сушу. Потенциальная энергия используется на гидроэлектростанциях, а химическая энергия долго оставалась без внимания.